编者按:近年来,人工智能(AI)与家用医疗设备的融合正在加速重塑眼科诊疗模式。其中,家用光学相干断层扫描(OCT)被认为是继抗VEGF药物问世之后,又一项改变新生血管性年龄相关性黄斑变性(nAMD)诊疗路径的重要技术。它让慢性眼病监测从"被动、间断"转变为"主动、持续",使医生能够实现远程精准管理。第129届美国眼科学会年会(AAO 2025)会议上,美国拉什大学医学中心Mathew MacCumber教授结合多项关键研究进展与典型病例,全面介绍了AI在家用OCT中的应用、临床成果以及未来发展方向。

家用OCT:延伸诊室边界的创新工具
传统nAMD管理依赖门诊定期OCT检查,但两次复诊之间通常间隔数周甚至数月,疾病活动可能在这段"空窗期"内悄然发生,导致患者错失最佳干预时机。家用OCT提供了突破性解决方案。患者可在家完成高质量眼底成像,影像通过加密方式上传云端,由AI系统自动分析与量化。医生无需面对面即可实时掌握患者眼内结构变化,实现从间断到连续的动态管理。
2022年发表于Ophthalmology Retina的前瞻性研究首次系统验证了Notal Vision家用OCT(NVHO)系统的临床可行性。研究由Liu、Holekamp与Heier等国际知名视网膜专家主导,15名nAMD患者在家中连续3个月每日自我成像。结果显示:
患者平均每周成功完成5.7次扫描,图像质量达标率高达97%;
AI分析系统(Notal OCT Analyzer, NOA)与人工判读的一致率达87%以上;
与门诊OCT对比,家用OCT测量的液体体积相关性高达r=0.92。
更重要的是,研究首次量化了视网膜液体体积的动态变化轨迹及其曲线下面积(AUC),揭示了个体在抗VEGF治疗响应速度、液体再积聚模式及治疗间期液体负荷方面的显著差异,为个体化疗程调控提供了科学依据。
临床实证:家用OCT显著延长治疗间隔
2024年发表于Retina的前瞻性干预试验直接证明了家用OCT的临床价值。该研究纳入15名患者(27只眼),在6个月内平均每周完成约6次家用OCT扫描,共获取4435张影像(91%可定量分析)。研究者将家用OCT的AI分析结果纳入治疗决策流程,结果令人振奋:
治疗间隔显著延长:从平均8周延长至15.3周,增幅达48%(P=0.004);
治疗负担明显降低:注射次数减少约43%;
视力保持稳定:最佳矫正视力(BCVA)在家用OCT指导管理前后无显著差异。
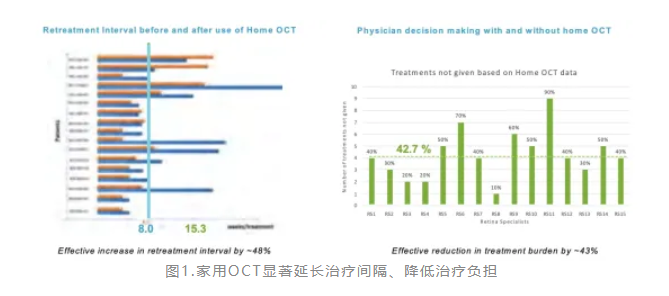
AI生成的液体体积动态轨迹清晰揭示了个体化的疾病活动模式与复发节律,帮助医生精准判断干预时机,实现真正的"按需治疗"策略优化。这是全球首个将家用OCT影像真正用于临床决策的实证试验,标志着远程自我成像结合AI分析已从"技术可能"迈向"临床实用"。
AI核心引擎:NOA获FDA批准
在家用OCT系统中,AI不是附属功能,而是核心引擎。患者每周产生的数十张OCT影像若依赖人工阅片,将耗费大量时间与人力。而AI算法能在数秒内完成三维图像的识别、分割与量化,将复杂的视网膜结构信息转化为直观的液体体积曲线。
NOA基于经典的U-Net编码器-解码器深度学习架构开发,这是医学图像分割领域最成熟的神经网络之一。U-Net的优势在于:它能在进行局部特征分割的同时保留整幅图像的全局结构信息,从而精准识别病灶区域并维持空间一致性。NOA算法可自动识别并测量视网膜中的低反射空间——这些区域通常提示nAMD相关的液体积聚。系统能够分别量化视网膜内液体(IRO/IRF)与视网膜下液体(SRO/SRF)的分布,并计算总视网膜低反射空间体积(TRO volume),以体积单位(VU)呈现。
2024年发表于Ophthalmology Science的研究是全球首个以FDA注册为目标的前瞻性验证试验。在387例nAMD患者中评估NOA性能:
高成像成功率:患者能在家中成功完成93.7%的自主成像;
优异的重复性:AI分析变异系数仅11.1%,优于人工的16.4%;
可靠的一致性:与人工判读的Dice系数中位数为0.68,达临床标准。
该研究以临床级数据和监管标准证实了AI驱动家用OCT系统的可行性与可靠性,标志着AI在OCT影像分析领域获得FDA批准的重要里程碑,为未来远程、个体化的眼科疾病管理奠定了坚实基础。
智能闭环:从居家成像到精准干预
家用OCT不仅仅是一台设备,而是一套完整的智能监测服务体系,构建了"居家成像—云端分析—医生决策—精准干预"的完整闭环。
患者自主成像:在家中定期使用家用OCT完成扫描;
AI实时分析:影像自动上传云端,NOA算法即时识别并量化视网膜内外液体,生成体积变化曲线;
智能预警触发:一旦液体体积超出医生预设阈值,系统自动推送警报;
远程决策干预:医生通过云端平台查看分析报告、投影图及病情轨迹,动态调整治疗方案。
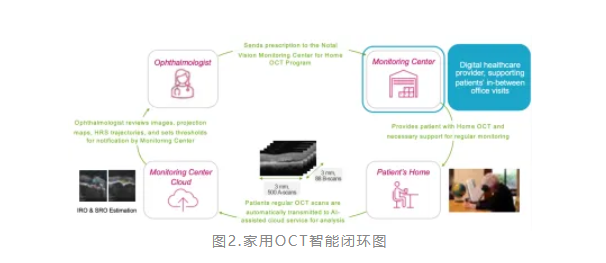
这一闭环管理模式将患者、医生与AI监测系统无缝连接,大幅提升了随访效率与疾病监测的连续性,实现了真正意义上的"早发现、早预警、早干预"。
真实病例:AI家用OCT的临床价值
患者基本情况:
75岁白人女性,2022年11月确诊新生血管性AMD(nvAMD)。初诊时右眼存在视网膜下液体(SRF),左眼结构稳定;基线视力为右眼20/50+1,左眼20/50-1。
随访治疗情况:
2022年12月1日(基线随访):确认左眼活动性nvAMD,接受抗VEGF药物注射治疗。
2022年12月3日(启动家用OCT):患者开始居家监测,液体体积维持在极低水平,治疗初期反应良好。
2023年1月18日(首次AI预警):家用OCT系统检测到SRF急剧上升,AI算法自动识别液体复发信号并触发警报。
2023年1月21日(及时干预):警报发出后3天内患者接受抗VEGF药物注射,视力改善至20/25-2;监测显示液体迅速回落。
2023年2月28日(中期随访):病情稳定,液体消退,视力进一步恢复至20/20。医生据此将患者纳入延长治疗间隔策略。
2023年3月22日(第二次预警):系统再次检测到液体上升,次日即进行抗VEGF药物注射,液体迅速消退,视力维持20/20-2。
该病例充分展示了AI辅助家用OCT系统的核心优势:实时监控捕捉疾病活动,早期预警避免视力损害,AI揭示个体化复发模式,减轻医患负担。
总结与展望
AI加持的家用OCT系统为慢性眼病管理带来了根本性变革:从"时间切片"到"时间曲线"的连续监测,从被动干预到AI预警的主动防控,从经验判断到量化数据的精准决策,从诊室检查到居家自测的便捷管理。随着算法优化和监管完善,其应用正从湿性AMD扩展至糖尿病黄斑水肿、视网膜静脉阻塞等更多慢性视网膜疾病。未来,结合5G通信与多模态数据整合,AI将实现疾病进展预测,从"被动干预"迈向"主动预防"。家用OCT有望像血糖仪一样普及,成为慢性眼病管理的标准工具,真正实现医疗从"治疗中心"向"患者中心"的转变,为全球数百万黄斑病变患者带来更安全、更便捷、更精准的治疗体验。让病变可视、让变化可量、让干预可控、让管理可持续——这就是AI驱动的家用OCT时代。
参考来源:AAO 2025官网
声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
2 comments






 京公网安备 11010502033360号
京公网安备 11010502033360号
条评论
Linda Gareth
2015年3月6日, 下午2:51Donec ipsum diam, pretium maecenas mollis dapibus risus. Nullam tindun pulvinar at interdum eget, suscipit eget felis. Pellentesque est faucibus tincidunt risus id interdum primis orci cubilla gravida.