编者按:2026年视觉与眼科研究协会年会(ARVO 2026)将于5月3日至7日在美国科罗拉多州丹佛市举办。作为全球眼科学与视觉研究领域规模最大、影响力最广的学术盛会,本届年会以“创新视觉研究引领精准眼科演进”为议题,聚焦如何整合干细胞研究、遗传学、基因编辑、人工智能和先进成像等前沿技术的突破,为眼部疾病的理解、诊断与治疗开辟新路径。此次会议上,开幕式与闭幕式将举行两场重磅主题演讲:诺贝尔化学奖得主Thomas R. Cech教授将以核酸疗法为核心,阐述基因治疗在眼科领域的最新进展;干细胞研究先驱Sally Temple教授将聚焦神经退行性疾病,展示再生医学在视觉健康领域的转化前景。这两场主题演讲的交汇将展现当代眼科学发展的新高度,影响眼科医学未来发展的深远影响。
5月3日,重磅开幕——诺奖得主预言:RNA将如何改写眼科治疗?
当地时间5月3日(星期日)上午10:15-11:45,1989年诺贝尔化学奖得主Thomas R. Cech教授将亲带来ARVO 2026开幕主题演讲:“A Farsighted Perspective on Nucleic Acid Therapeutics for Eye Disease”。
随着mRNA疫苗的成功应用和CRISPR基因编辑技术的发明,核酸疗法正站在一个关键的十字路口。在这个充满未知的时刻,我们不禁思考:RNA将成为医学领域的主流范式,还是其应用将受到更多限制?在本次主题演讲中,Thomas R. Cech教授将首先以其新书The Catalyst: RNA and the Quest to Unlock Life’s Deepest Secrets(W.W. Norton出版)中的案例为例,回顾RNA研究的重大发现。随后,他将探讨核酸疗法在治疗遗传性眼病方面的潜力,包括Leber先天性黑矇(LCA)和年龄相关性黄斑变性(AMD)。与传统小分子药物相比,核酸疗法既展现出独特优势,也面临着新的挑战。
Thomas R. Cech教授简介

Thomas R. Cech教授在加州大学伯克利分校获得化学博士学位,并在麻省理工学院完成博士后研究,随后加入科罗拉多大学博尔德分校任教。他于1988年成为霍华德·休斯医学研究所(HHMI)研究员,并于1990年晋升为化学与生物化学特聘教授。
1982年,Thomas R. Cech教授及其研究团队宣布,从池塘微生物四膜虫中提取的一种RNA分子能够催化生化反应。这一发现首次打破了"只有蛋白质才能作为酶"的长期共识,这使其与耶鲁大学的Sidney Altman教授共同赢得1989年诺贝尔化学奖。
2000年1月,Thomas R. Cech教授出任美国最大的私立生物医学研究机构HHMI主席,迁至马里兰州。2009年,他重返科罗拉多大学博尔德分校,继续从事科研与教学工作,并担任BioFrontiers研究所创始主任直至2020年。
Thomas R. Cech教授始终致力于向公众传播科学知识,为此撰写的The Catalyst一书被 The Economist 评为2024年度最佳图书之一。他获得的荣誉还包括:荷兰皇家艺术与科学学院海尼根奖(1988年)、加拿大盖尔德纳国际奖(1988年)、阿尔伯特·拉斯克基础医学研究奖(1988年)以及美国国家科学奖章(1995年)。1987年,他当选美国国家科学院院士,并获美国癌症学会终身教授荣誉。2000年,他入选美国国家医学院。
5月7日,闭幕演讲——干细胞治疗实现历史性突破
当地时间5月7日(星期四)上午10:15-111:30,神经干细胞研究所科学主任Sally Temple教授将带来ARVO 2026闭幕主题演讲:“Modeling, Targeting, and Healing: Stem Cell Strategies to Combat Neurodegeneration in the Brain and Eye”。
年龄相关性神经退行性疾病的攻克,亟需能够反映人类病理特征的先进研究模型,以深入解析疾病机制并推动治疗策略创新。Sally Temple教授团队提出了三种相互关联的干细胞技术应用策略,分别针对额颞叶痴呆(FTD-tau)、阿尔茨海默病(AD)和AMD的诊疗难点。
首先,Sally Temple教授团队建立了一套可规模化制备高质量大脑皮层类器官的方案,并运用该模型揭示了FTD-tau的致病机理。基于此,构建了全人源双功能抗tau-PEST胞内抗体,其能够有效降解毒性tau蛋白并显著提升神经元存活率,从而验证了靶向tau蛋白降解策略的治疗潜力。其次,通过构建人类脑血管细胞多组学图谱,发现AD风险基因APOE4会导致血管屏障功能障碍并诱发促炎状态。在iPSC来源的FTD-tau神经血管共培养模型中,抑制JAK-STAT信号通路可逆转APOE4引起的病理损伤,为该靶点的临床转化提供了直接依据。最后,针对AMD的治疗瓶颈,Sally Temple教授团队基于对视网膜色素上皮(RPE)干细胞的研究突破,成功研发出RPESC-RPE-4W(一种用于RPE细胞替代治疗的有丝分裂后祖细胞产品)。正在进行的首次人体临床试验显示,RPESC-RPE-4W植入治疗干性AMD表现出良好的安全性与耐受性,部分受试者视力平均提升达21.67个字母。
这一三位一体的转化研究体系,有机整合了干细胞脑类器官(针对FTD-tau)、多组学生物信息学(针对AD)及RPESC祖细胞技术(针对AMD)等前沿突破。从机制解析到临床干预的全链条研究进程中,人工智能(AI)的赋能作用贯穿始终:运用AI技术在全基因组关联分析中挖掘关键靶点、模拟复杂药物相互作用,并优化RPE祖细胞的标准化生产工艺。随着AI技术的持续演进,神经退行性疾病治疗研发进程有望实现跨越式加速。
Sally Temple教授简介

在神经干细胞研究所,Sally Temple教授主导的研究聚焦于干细胞在中枢神经系统发育、稳态维持与损伤修复中的作用机制。她在英国剑桥大学获得发育神经科学学士学位,随后于伦敦大学学院取得视神经发育博士学位。在迈阿密大学从事博士后研究期间,她在胚胎期哺乳动物中枢神经系统中鉴定出干细胞的存在,这一碑工作为神经干细胞研究领域奠定了重要基石。因其开创性贡献,Sally Temple教授荣获麦克阿瑟天才奖。
Sally Temple教授曾担任国际干细胞研究学会主席及理事,并当选美国国家医学院院士。她目前的研究横跨基础与转化神经科学领域,其中与丈夫Jeffrey Stern教授共同领导的临床阶段项目致力于开发针对AMD的干细胞疗法;同时,她通过建立患者来源的干细胞模型,系统研究AMD与tau蛋白病的发病机制,以推动再生治疗策略的创新突破。
更多ARVO 2026前沿动态
敬请持续关注
《国际眼科时讯》的后续报道!
来源:ARVO 2026官网
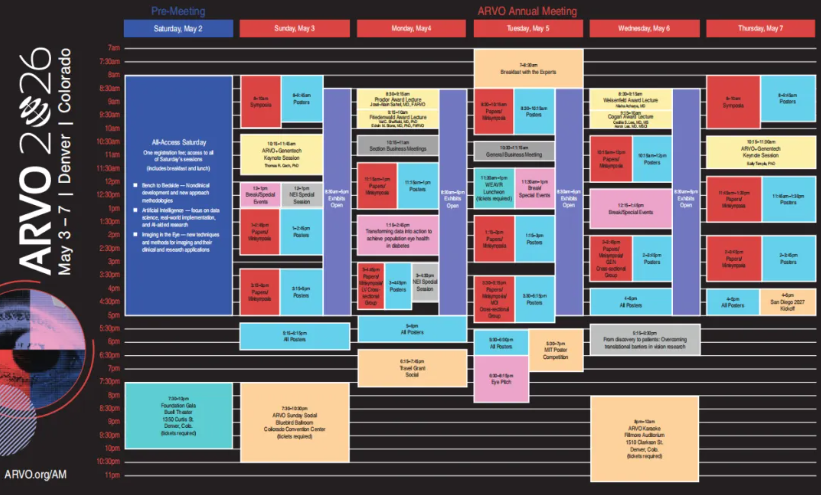
附:ARVO 2026日程速览
声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
2 comments
 京公网安备 11010502033360号
京公网安备 11010502033360号
条评论
Linda Gareth
2015年3月6日, 下午2:51Donec ipsum diam, pretium maecenas mollis dapibus risus. Nullam tindun pulvinar at interdum eget, suscipit eget felis. Pellentesque est faucibus tincidunt risus id interdum primis orci cubilla gravida.