编者按:间歇性外斜视是儿童与青少年中高发的眼科疾病,尤其在亚洲人群患病率显著。其病情进展可能伴随眼位控制能力下降与双眼视功能受损,而背后的大脑结构变化机制尚待深入揭示。在第十九届中国医师协会眼科医师分会年会(COA 2025)上,首都医科大学附属北京同仁医院付晶教授,围绕“基本型间歇性外斜视儿童和青少年的灰质微结构异常改变”这一主题,分享其团队运用离散度与密度成像(Neurite Orientation Dispersion and Density Imaging,NODDI)技术在该疾病脑机制研究中的最新发现,以期从脑结构视角进一步揭示IXT的神经病理基础,为临床诊治提供新思路。

间歇性外斜视(intermittent exotropia,IXT)是儿童最常见的眼科疾病之一,其患病率在美国约为1%s[1],在亚洲则高达4%[2]。在IXT的多种亚型中,基本型占主导地位,约占全部病例的86.2%[3]。该疾病随病情进展,患者的眼位控制能力会逐渐减弱,导致眼位偏斜加剧,并损害双眼单视功能。眼位与融合功能的维持,依赖于参与视觉信息传入、整合及眼球运动的各脑区在结构与功能上的正常及其间的协调配合。任何相关脑区的功能或结构改变,均可能干扰视觉通路或双眼融合功能的正常发育,从而推动IXT进展,加重眼位偏斜与立体视损害。
目前IXT的具体发病机制尚未完全阐明。最近研究发现,IXT儿童存在与融合功能和眼球运动相关的中枢结构异常[4],此外Fei等人也发现IXT患儿涉及视觉及眼球运动信号处理相关脑区——例如右侧额叶眼动区(frontal eye field,FEF)和双侧顶下小叶——出现灰质密度降低,而顶下小叶、右侧V4区和FEF的皮层厚度有所增加[5]。进一步借助弥散张量成像(diffusion tensor imaging,DTI),Zhu等人观察到IXT儿童右侧中央前回和右侧中央后回的各向异性(fractional anisotropy,FA)值显著降低,并且与IXT病程及斜视度呈负相关,提示这些区域白质微结构异常可能对IXT患者的眼球运动控制能力和双眼融合产生不利影响[6]。运用自动化纤维束量化分析(Automated fiber quantification analysi,AFQ),Guo也证实了IXT患者特定视觉相关纤维束存在微结构定量改变,这很可能导致其视觉信息处理困难[7]。
虽然DTI及扩散峰度成像(DKI)是探究大脑微结构常用的技术,但它们无法精准捕捉受限的非高斯扩散,且对不同扩散池缺乏特异性[8]。而神经突方向离散度与密度成像NODDI作为一种创新的多室扩散加权模型,能通过方向分散指数(the orientation dispersion index,ODI)、各向同性体积分数(the isotropic volume fraction,ISOVF)和细胞内体积分数(the intra-cellular volume fraction,ICVF)等多个定量指标,更细致地评估神经轴突和树突等大脑微结构[9-11]。相较于DTI与DKI,NODDI能更详尽地描绘脑发育状况,并通过更准确地刻画水分子在组织微环境内的扩散来阐明神经病理机制[12]。
研究方法
本研究为一项横断面设计,获首都医科大学北京同仁医院伦理委员会及机构审查委员会批准(批准号:TRECKY2020-139)。所有受试者及其监护人均签署书面知情同意书。研究纳入2021年5月至2023年8月于北京同仁医院斜视与小儿眼科就诊的基本型间歇性外斜视患者和正常志愿者,其中基本型IXT 组31人,健康对照组37人,两组在年龄、性别、利手和教育程度无显著差异。本研究纳入的受试者年龄在8~16岁,最佳矫正视力≥1.0,主要排除标准包括患有其他类型斜视、存在弱视或屈光参差等双眼视功能异常、有青光眼或视神经炎病史、存在精神或脑部疾病史、有眼部或脑部手术史,以及存在MRI扫描禁忌症等。
所有受试者均接受3.0 T MRI扫描,序列包括高分辨率三维T1加权结构像和扩散谱成像(DSI)。扫描过程中使用泡沫垫固定头部以减少运动,并以耳塞降低噪音干扰。DSI序列采用多b值设计(0-3000 s/mm²),以获取更全面的水分子扩散信息。同时完成蒙特利尔认知评估(MoCA)与详细的眼科检查,比如斜视度测量(三棱镜交替遮盖试验)、立体视(随机点立体图)、三级视功能(同视机)及斜视控制能力(Newcastle控制评分)。
数据处理遵循标准化流程。首先对原始扩散数据进行涡流矫正和头动校正等预处理。随后,使用基于Python的Dipy工具包进行神经突方向离散度与密度成像模型重建,分别生成反映神经突密度的细胞内体积分数图、表征纤维方向一致性的方向分散指数图以及代表自由水成分的各向同性体积分数图。为进一步分析,将每个个体的T1加权像与b0图像进行配准,并利用由此得到的变换矩阵,将所有NODDI参数图归一化至标准的MNI空间,以实现所有参与者数据间的体素级对齐。最后,基于解剖自动标记图谱,提取包括初级视觉皮层、高级视觉相关皮层、眼球运动控制脑区及认知相关区域在内的多个感兴趣区的平均参数值,用于后续的组间比较与相关分析。
统计分析使用SPSS 25.0软件。组间人口统计学特征比较采用双尾t检验或Fisher精确检验。采用两独立样本t检验比较IXT组与HC组间各脑区NODDI参数的差异。采用Pearson或Spearman相关分析探究IXT组内差异脑区参数与临床特征(如斜视度、病程)的相关性。所有检验均为双尾,P < 0.05视为具有统计学显著性。
研究结果与讨论
本研究纳入31例基本型IXT患儿,平均年龄为10.94 ± 1.69岁,男性16人,女性15人;正常对照组37人,平均年龄为10.94 ± 1.69岁,男性23人,女性14人。
ODI值主要与轴突扇形分布方向有关,ODI越高,说明分散性越大,更趋于扇形分布,ODI值越低,说明轴突分布越集中;ICVF主要表示神经密度,ICVF降低表明神经密度减少;ISOVF主要与细胞外自由水相关,ISOVF增加与细胞外水肿和神经炎症有关,ISOVF降低可能与细胞增殖相关。
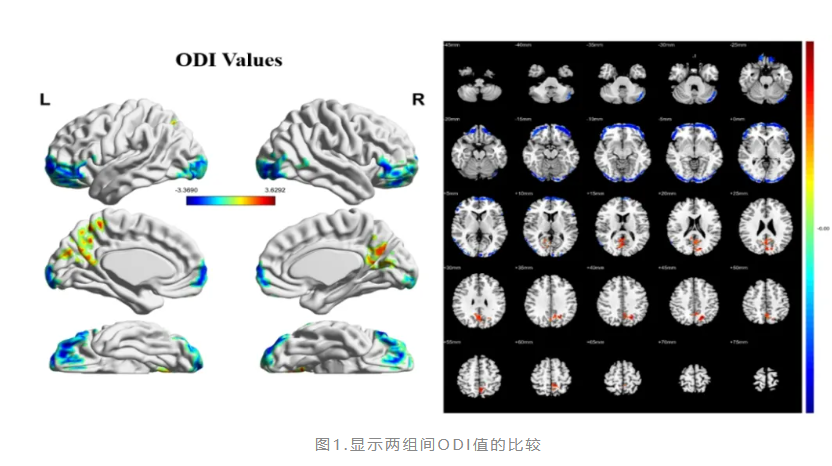
与正常对照组相比,IXT儿童在与视觉感知和双眼视功能相关的大脑区域显示出较低的ODI值,包括双侧舌回、距状裂、枕下回、枕中回、左侧颞中回和双侧眶额皮层。而在双侧楔前叶和左楔叶、枕上回和缘上回中发现ODI值增加(图1)。
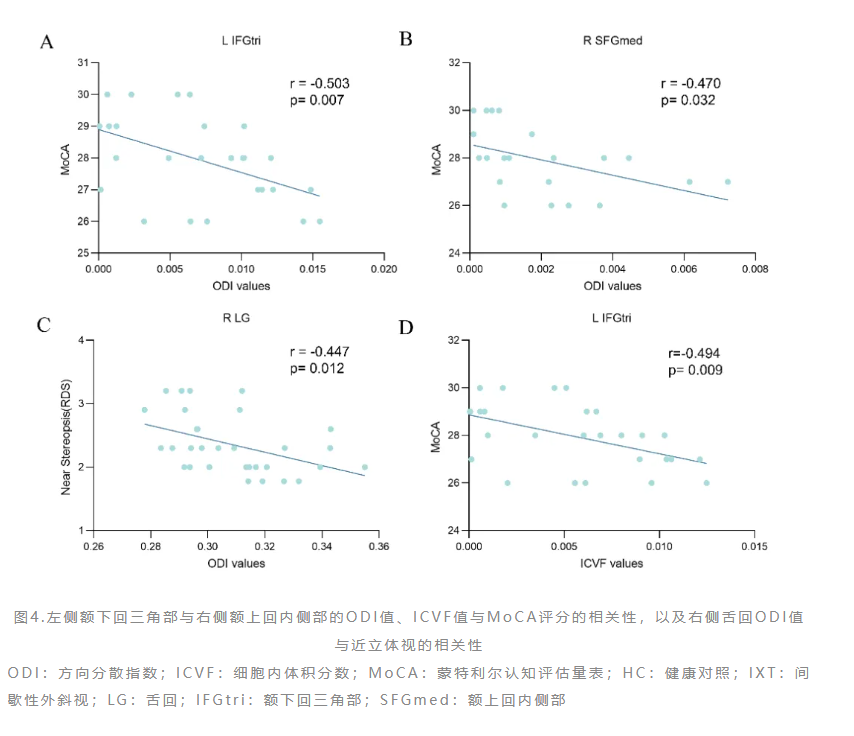
本研究发现的上述脑区微结构异常,与既往功能影像学研究相互印证。例如,Fei等人报道基本型IXT儿童左侧舌回和右侧枕下回的低频波动振幅降低,提示其视觉空间注意与记忆功能可能受损[5]。此外,参与立体视和空间信息处理的枕中回[13,14]、负责三维视觉运动的颞中回[15],以及与视觉识别和高级信息整合密切相关的眶额皮层[16],在本研究中均显示出微结构改变。这与先前在共同性斜视成人患者中观察到的眶额皮层皮质变薄[17]及颞中回灰质/白质体积减少[18]等结构性异常相一致,提示轴突组织紊乱可能导致相关脑区功能障碍及发育异常。值得注意的是,本研究还发现右侧舌回的轴突方向分散指数(ODI)值与近立体视锐度呈负相关(图4),即ODI降低(轴突方向一致性增高)伴随近立体视恶化。此外,在双侧楔前叶、左侧楔叶、枕上回及顶上回等视觉相关皮层,本研究观测到ODI值升高,提示这些区域可能存在轴突方向一致性降低。这些脑区分别涉及视觉-前庭整合[19]、高级视觉联合处理[20]以及眼动和空间信息加工[21]。这意味着高级视觉相关皮层轴突连贯性丧失,而神经突起密度保持不变。
此外,我们发现IXT儿童在双侧额中回和额部眶内侧回中表现出较低的ODI、ICVF和ISOVF值(图1-3),在涉及眼球运动控制区的双侧小脑中表现出更低的ODI和ISOVF值(图1、3)。这些区域出现的轴突密度丧失、轴突连贯性增加和异常的神经元细胞增殖[22](以较低的ISOVF为指标)可能与IXT患者的眼球运动控制能力受损有关。我们的研究揭示了IXT患者眼球运动和视觉感知相关的脑区微观结构异常的不同模式。眼球运动相关脑区显示出ODI、ICVF和ISOVF的变化,而与视觉感知相关的大脑区域仅表现出ODI值的改变,同时既往研究表明轴突连贯性的改变可能先于神经突起密度的丧失[11]。因此与视觉感知相关的脑区相比,眼球运动相关脑区的微观结构异常更为严重,这表明IXT患者可能会在眼球运动中枢经历更早的微观结构变化。
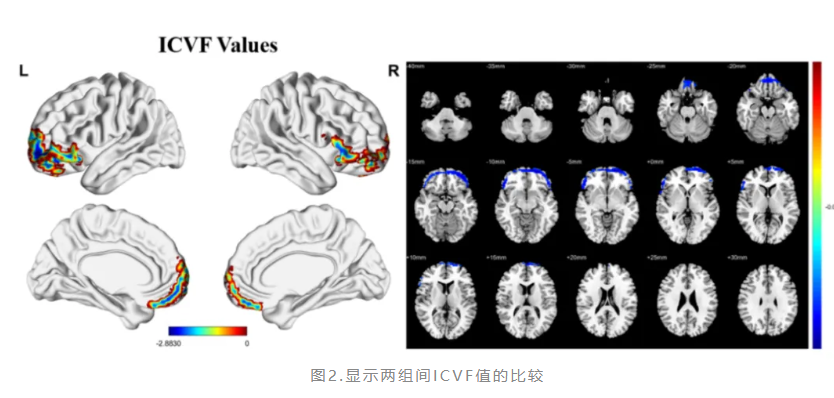
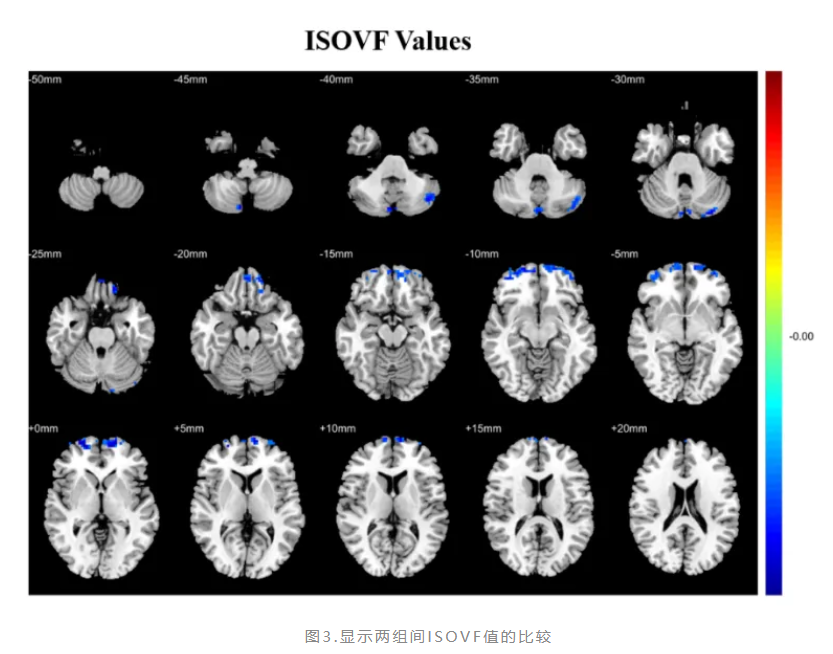
同时,我们还发现与认知和情绪管理相关的双侧额上回ODI、ICVF和ISOVF值降低(图1-3),以及双侧额下回ODI和ICVF值降低(图1、2)。额上回的眶部不仅在情绪调节中起关键作用,还涉及人际关系和复杂社交活动[23]。额下回是情绪与认知控制环路的关键脑区,参与情感过程和认知控制[23,24]。既往研究显示,有自杀风险的抑郁个体右侧额下回眶部的灰质体积(GMV)减少[25]。因此可以推测这些区域的微结构异常可能与IXT患者的认知和情绪处理障碍相关。我们还发现蒙特利尔认知评估量表(MoCA)评分与右侧内侧额上回和左侧三角部额下回的ODI值以及ICVF值呈负相关(图4),这表明内侧额上回和三角部额下回的轴突一致性丧失及神经突密度改变可能影响IXT患者的认知功能。MoCA评分可作为评估IXT患者情绪管理和认知功能的生物标志物。
研究结论
综上所述,基本型间歇性外斜视患儿在与视感知觉、眼球运动、认知及情绪管理相关的多个脑区存在灰质微结构改变,且相较于视感知觉相关脑区,IXT患者可能更早经历眼球运动中枢的微结构变化。此外,近立体视锐度和蒙特利尔认知评估量表评分分别与视觉感知和认知情绪管理相关脑区的微结构改变呈负相关。这些指标可作为评估IXT患者病情严重程度及认知变化的重要生物标志物。本研究通过神经突方向离散度与密度成像技术,揭示了间歇性外斜视发生机制的重要中枢机制线索,为深入理解该疾病的病理生理基础提供了关键新知。
参考文献
[1]Govindan M, Mohney B G, Diehl N N, et al. Incidence and types of childhood exotropia: a population-based study [J]. Ophthalmology, 2005, 112(1): 104-8.
[2]Fu J, Li S M, Liu L R, et al. Prevalence of amblyopia and strabismus in a population of 7th-grade junior high school students in Central China: the Anyang Childhood Eye Study (ACES) [J]. Ophthalmic Epidemiol, 2014, 21(3): 197-203.
[3]Kim D H, Jung J H, Choi M Y, et al. A cross-sectional study of ophthalmologic examination findings in 5385 Koreans presenting with intermittent exotropia [J]. Sci Rep, 2023, 13(1): 1329.
[4]Zhang W, Fei N, Wang Y, et al. Functional changes in fusional vergence-related brain areas and correlation with clinical features in intermittent exotropia using functional magnetic resonance imaging [J]. Hum Brain Mapp, 2023, 44(15): 5002-12.
[5]Fei N, Wang Y, Yang B, et al. Structural and spontaneous functional brain changes in visual and oculomotor areas identified by functional localization task in intermittent exotropia children [J]. Brain Res, 2023, 1819: 148543.
[6]Zhu H, Guo W, Wu Q, et al. Structural and Functional Changes of Brain in Children With Intermittent Exotropia: A Study Combining Multiple MRI Modalities [J]. J Neuroophthalmol, 2023.
[7]Guo J, Zhou L, Wang Y, et al. Automated fiber quantification analysis identifies tract-specific microstructural alterations in brain in intermittent exotropia [J]. Brain Res Bull, 2024, 219: 111113.
[8]Pines A R, Cieslak M, Larsen B, et al. Leveraging multi-shell diffusion for studies of brain development in youth and young adulthood [J]. Dev Cogn Neurosci, 2020, 43: 100788.
[9]Gozdas E, Fingerhut H, Dacorro L, et al. Neurite Imaging Reveals Widespread Alterations in Gray and White Matter Neurite Morphology in Healthy Aging and Amnestic Mild Cognitive Impairment [J]. Cereb Cortex, 2021, 31(12): 5570-8.
[10]Slattery C F, Zhang J, Paterson R W, et al. ApoE influences regional white-matter axonal density loss in Alzheimer's disease [J]. Neurobiol Aging, 2017, 57: 8-17.
[11]Haykal S, Invernizzi A, Carvalho J, et al. Microstructural Visual Pathway White Matter Alterations in Primary Open-Angle Glaucoma: A Neurite Orientation Dispersion and Density Imaging Study [J]. AJNR Am J Neuroradiol, 2022, 43(5): 756-63.
[12]Luo Y Q, Liang R B, Xu S H, et al. Altered regional brain white matter in dry eye patients: a brain imaging study [J]. Aging (Albany NY), 2022, 14(6): 2805-18.
[13]Zhu P W, Huang X, Ye L, et al. Altered intrinsic functional connectivity of the primary visual cortex in youth patients with comitant exotropia: a resting state fMRI study [J]. Int J Ophthalmol, 2018, 11(4): 668-73.
[14]Fortin A, Ptito A, Faubert J, et al. Cortical areas mediating stereopsis in the human brain: a PET study [J]. Neuroreport, 2002, 13(6): 895-8.
[15]Xu J, Wang J, Fan L, et al. Tractography-based Parcellation of the Human Middle Temporal Gyrus [J]. Sci Rep, 2015, 5: 18883.
[16]Kveraga K, Boshyan J, Bar M. Magnocellular projections as the trigger of top-down facilitation in recognition [J]. J Neurosci, 2007, 27(48): 13232-40.
[17]Yin X, Chen L, Ma M, et al. Altered Brain Structure and Spontaneous Functional Activity in Children With Concomitant Strabismus [J]. Front Hum Neurosci, 2021, 15: 777762.
[18]Ouyang J, Yang L, Huang X, et al. The atrophy of white and gray matter volume in patients with comitant strabismus: Evidence from a voxel-based morphometry study [J]. Mol Med Rep, 2017, 16(3): 3276-82.
[19]Liu L Q, Li Q Y, Zhang Z H, et al. Altered functional connectivity of primary visual cortex in adults with strabismus and amblyopia: a resting-state fMRI study [J]. J Integr Neurosci, 2022, 21(1): 4.
[20]Uddén J, Snijders T M, Fisher S E, et al. A common variant of the CNTNAP2 gene is associated with structural variation in the left superior occipital gyrus [J]. Brain Lang, 2017, 172: 16-21.
[21]Min Y L, Su T, Shu Y Q, et al. Altered spontaneous brain activity patterns in strabismus with amblyopia patients using amplitude of low-frequency fluctuation: a resting-state fMRI study [J]. Neuropsychiatr Dis Treat, 2018, 14: 2351-9.
[22]Hagiwara A, Kamagata K, Shimoji K, et al. White Matter Abnormalities in Multiple Sclerosis Evaluated by Quantitative Synthetic MRI, Diffusion Tensor Imaging, and Neurite Orientation Dispersion and Density Imaging [J]. AJNR Am J Neuroradiol, 2019, 40(10): 1642-8.
[23]Kuusinen V, Cesnaite E, Per?kyl? J, et al. Orbitofrontal Lesion Alters Brain Dynamics of Emotion-Attention and Emotion-Cognitive Control Interaction in Humans [J]. Front Hum Neurosci, 2018, 12: 437.
[24]Kokudai Y, Honma M, Masaoka Y, et al. Cascade process mediated by left hippocampus and left superior frontal gyrus affects relationship between aging and cognitive dysfunction [J]. BMC Neurosci, 2021, 22(1): 75.
[25]Yang Y, Chattun M R, Yan R, et al. Atrophy of right inferior frontal orbital gyrus and frontoparietal functional connectivity abnormality in depressed suicide attempters [J]. Brain Imaging Behav, 2020, 14(6): 2542-52.
声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
2 comments


 京公网安备 11010502033360号
京公网安备 11010502033360号
条评论
Linda Gareth
2015年3月6日, 下午2:51Donec ipsum diam, pretium maecenas mollis dapibus risus. Nullam tindun pulvinar at interdum eget, suscipit eget felis. Pellentesque est faucibus tincidunt risus id interdum primis orci cubilla gravida.