Leber 遗传性视神经病变(LHON)是一种由线粒体 DNA 突变(mtDNA)导致、呈母系遗传的罕见致盲性眼病[1]。该病起病隐匿、进展迅猛,传统以维生素、激素为主的支持治疗效果十分有限,多数患者确诊后便陷入“有诊断、无治疗”的绝望困境,给家庭与社会带来沉重负担。然而,科学的进步从未停止。2015年,全球首款且迄今唯一获批的LHON治疗药物——艾地苯醌(Raxone™,150mg)上市,标志着该疾病治疗从"对症支持"迈入"对因干预"的精准医学时代。该药物通过绕过受损的线粒体复合物I、恢复细胞ATP合成并抑制氧化应激,为LHON患者带来了重获光明的可能。但临床实践中,一个现象常常困扰着医患双方:部分患者在启动治疗后,视力并未立即直线上升,反而可能出现短暂的波动甚至进一步下降。这一现象是否意味着"治疗失败"? 答案是否定的。本刊特邀首都医科大学附属北京同仁医院姜利斌教授结合最新临床研究证据,系统阐述LHON的疾病本质与动态病程,深度解读治疗中出现的"谷底-恢复"现象,并阐明坚持长期治疗(≥18-24个月)对于实现视力最大化恢复的深远意义。
流行病学概览
十万之众的青壮年视力“隐形杀手”
LHON在我国并非“极罕见”。数据显示,我国累计患者人数已超过十万,构成了不容忽视的疾病负担[2]。该病具有鲜明的流行病学特征:约90%的患者为15~35岁的男性青壮年[3],正值个人发展与社会贡献的关键时期,因此疾病对患者个人、家庭及社会的影响尤为深远。此外,该疾病临床进程极具侵袭性:典型表现为急性 / 亚急性、无痛性中心视力丧失,双眼通常先后发病,间隔仅数周至数月。自然病程中,患者视力在发病后6 个月内快速进展至重度受损。在基因分型方面,根据LEROS研究(2024)[4],全球范围内约90%的LHON患者携带m.11778G>A、m.3460G>A、m.14484T>C三大常见mtDNA突变,该比例在不同地区存在差异,如中国人群中m.11778G>A突变占比高达85%,是最主要的致病类型;而在部分中国队列中,三大常见突变占比仅约40%,其余为罕见突变类型。同时,作为母系遗传疾病,LHON 还存在家族传递风险,亚洲人群散发病例占比达 40%~50%,进一步增加了早期筛查与干预的难度[5]。
发病机制解密
线粒体能量“断供”与RGCs的“静默”
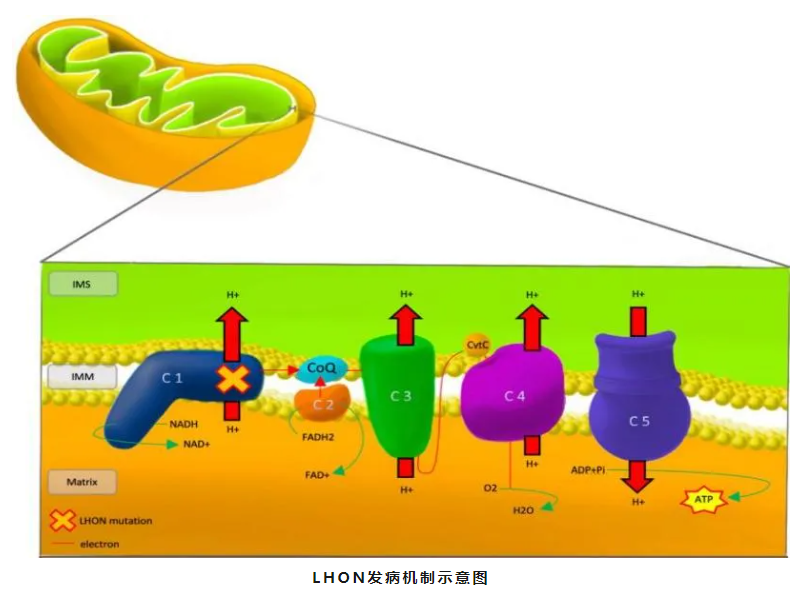
LHON 的本质是线粒体呼吸链功能衰竭引发的视网膜神经节细胞(RGCs)退行性病变,核心病因是mtDNA原发突变。目前已明确,m.11778G>A、m.14484T>C、m.3460G>A三大突变类型可直接靶向线粒体呼吸链复合物I,导致其结构异常,电子传递功能严重受损。这一分子缺陷进一步触发级联式病理损伤[6]:
三磷酸腺苷(ATP)合成锐减
复合物I是电子进入呼吸链的核心入口,其功能失能导致下游质子梯度建立受阻,最终ATP生成量显著下降,高能耗的RGCs对此尤为敏感;
氧化应激风暴级联放大
电子在阻滞位点大量泄漏,与分子氧结合生成过量活性氧,引发脂质过氧化、蛋白质羰基化及DNA双链损伤;
RGCs进入"功能性静默"与渐进性凋亡
能量匮乏与氧化损伤的双重打击下,RGCs轴突肿胀、线粒体空泡化,细胞并非即刻坏死,而是进入一种"结构残存、功能沉默"的代偿性休眠状态;若损伤持续存在,则最终走向不可逆凋亡,形成视神经萎缩。
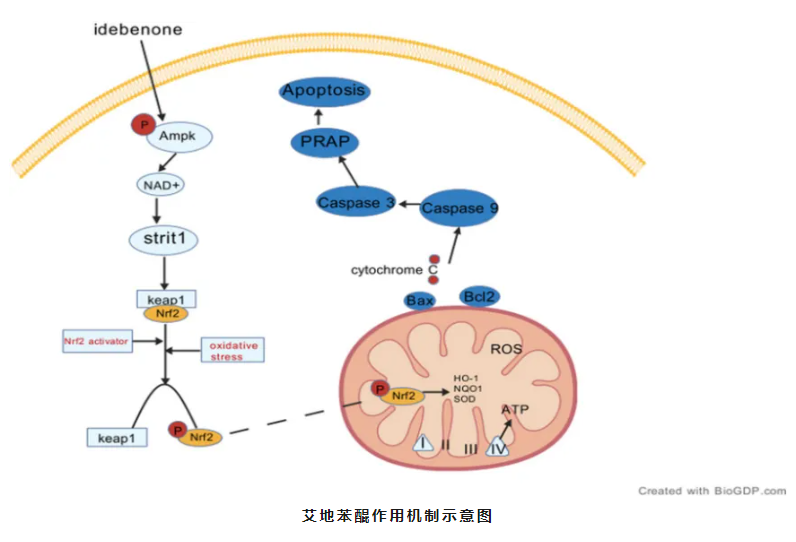
在上述病理链条中,艾地苯醌的作用靶点精准而独特:它是一种人工合成的短链苯醌类化合物。作为外源性电子载体,艾地苯醌可接受复合物I上游的电子,并将其直接递送至复合物III,从而绕过受损的复合物I,恢复下游电子传递与ATP合成;同时,其醌/氢醌结构可在氧化态与还原态之间可逆转换,不仅能够直接清除ROS、抑制脂质过氧化,还可调控花生四烯酸代谢通路,抑制环氧合酶与脂氧合酶活性,从源头阻断"氧化应激-能量耗竭"的恶性循环。这种"双轨并行"的作用机制,使其不仅能够保护残存RGCs免于进一步损伤,更能够为处于"休眠状态"、结构尚且完整的RGCs细胞提供能量支持与抗氧化保护,促使其功能逐步复苏——这正是长期治疗实现持续视力改善的生物学基础[7-8]。
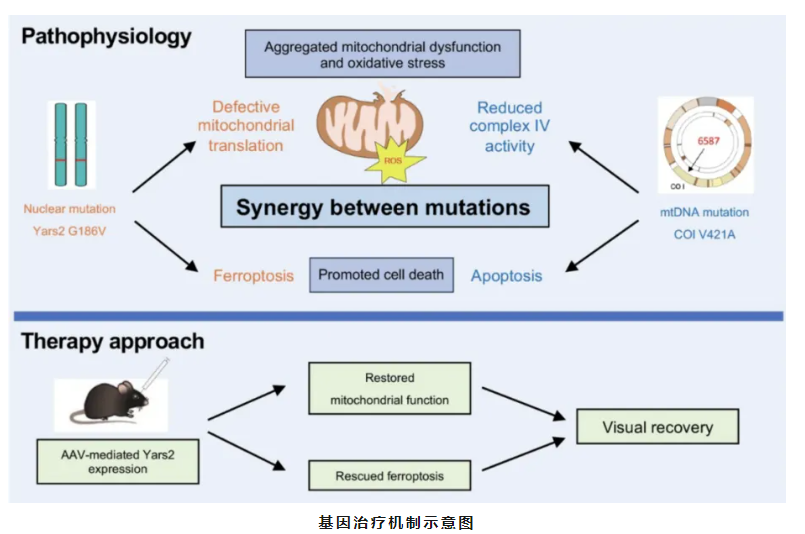
值得强调的是,LHON并非单纯"单基因决定论"疾病。浙江大学遗传学研究所管敏鑫教授团队已通过研究证实,核基因修饰效应与线粒体单体型共同构成关键的"外显率调控网络":例如,核基因YARS2(编码线粒体酪氨酰-tRNA合成酶)的特定变异可显著降低m.11778G>A突变携带者的发病风险;而东亚人群高发的线粒体单体型M7b则与疾病易感性升高相关[9]。这进一步明确LHON是遗传背景与环境因素共同作用的复杂性疾病,为个体化风险评估与干预提供了分子基础。
自然病程与治疗中的动态演变
"谷底"是走向"恢复"的可预期生理阶段
理解LHON的治疗,必须首先尊重其固有自然病程。扩大准入计划(EAP)研究[10]中引用的自然史数据清晰显示:未经治疗的LHON患者,视力恶化具有明确的速度与趋势。超过70%的患者在症状出现后3个月内即可进展至法定盲水平(BCVA >1.0 logMAR);而自发视力恢复极为罕见,尤其对于占比最高的m.11778G>A突变,其自然恢复率不足10%(RHODOS研究[11]安慰剂组10.3%,自然史研究31.1%为所有突变类型综合数据),多数患者视力将永久停滞于极低水平。
然而,经艾地苯醌治疗后,患者的病程并未如想象中的简单"刹车"或"逆转",而是呈现出动态波折的演进过程。EAP研究对87例入组患者的纵向追踪,首次在真实世界场景中系统描绘了这一动态图景:
"谷底"的普遍性与可预期性
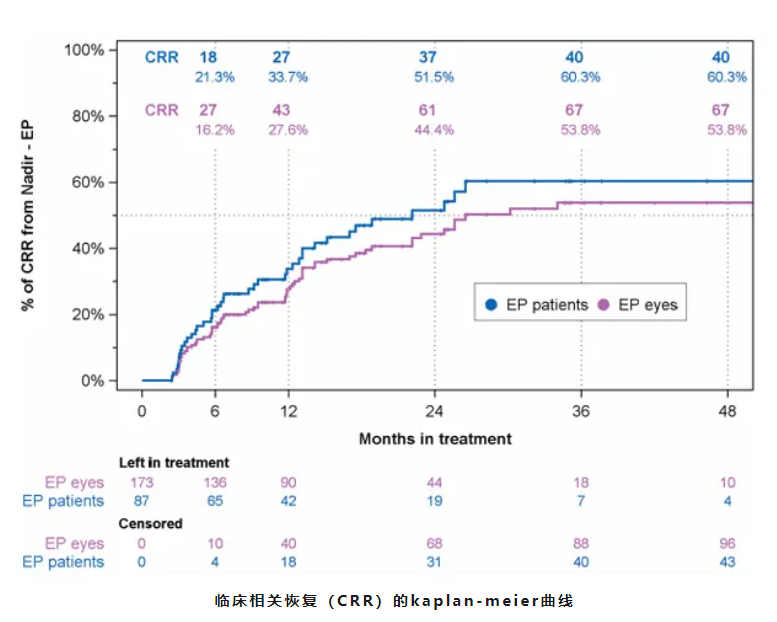
部分患者启动治疗后,视力并未立即改善,反而在3–6个月内出现一过性进一步下降,达到病程谷底值(Nadir)。数据显示,在最终实现临床相关恢复(CRR)的67只眼中,49.7%(86/173)在“谷底”阶段已处于超视力状态(BCVA >1.68 logMAR,即无法辨认ETDRS视力表上任何字母)[10]。这绝非治疗失败的信号,而是疾病固有进展惯性与药物起效所需生物学时间相互作用的必然结果——药物需要时间渗透至视神经组织、累积至有效浓度、启动线粒体功能修复程序,在此期间,尚未得到保护的RGCs仍可能经历最后的损伤性"滑坡"。
"恢复"的延迟性与累积性
视力改善绝非立竿见影。EAP数据显示,首次观察到CRR的中位时间为9.5个月(范围2.5–26.5个月)。"谷底"阶段时,仅9.2%的患者视力优于20/200,44.8%的患者视力降至极差(off-chart)水平。末次随访时,32.2%的患者视力恢复至优于20/200,整体视力较谷值显著改善[10]。更重要的是,患者从首次CRR到末次随访,视力改善幅度从平均0.45 logMAR(约22个ETDRS字母)显著增加至0.72 logMAR(约36个ETDRS字母)[10]。这一动态曲线有力证明:"恢复"不是一次性临床事件,而是需要足够时间窗完成的渐进式神经功能重建过程。此外,RHODOS研究[11]因治疗周期仅6个月,未能充分捕捉艾地苯醌的长期疗效,仅观察到视力改善趋势,未达到统计学显著性,这也进一步印证了短期治疗无法评判LHON疗效的观点。
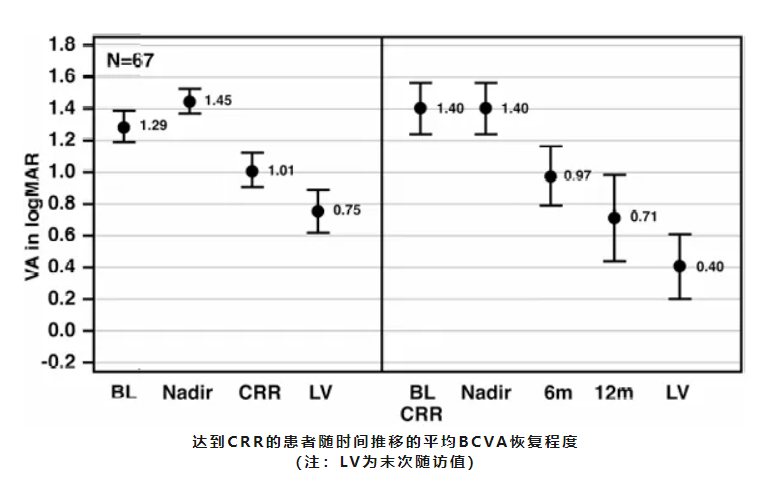
因此,临床应当理性认知而非恐惧"谷底",它是疾病动态演进中一个可预期、可跨越的生理节点。以短期(如3–6个月)视力变化评判艾地苯醌疗效,无异于在种子破土前否定其生命力,既不科学,也不公正。
治疗过程与循证证据
长期坚持,方能静待"光"来
EAP研究提供的长期真实世界数据(平均治疗25.6个月),为上述动态过程和长期治疗的必要性提供了实证基石。该研究证实了艾地苯醌治疗的双重获益维度,即:
逆转视力丧失
46.0%的患者实现了CRR(临床相关恢复,定义为:从脱靶视力[off-chart]恢复至在ETDRS视力表上可辨认至少1行[5个字母],或在靶上视力[on-chart]基础上改善至少2行[10个字母])[10];
冻结疾病进展
在治疗初期尚存有用视力(BCVA < 1.0 logMAR)的患者中,50%成功地将视力稳定在该阈值之上(CRS),避免了向法定盲水平的滑落,部分患者视力甚至获得改善。
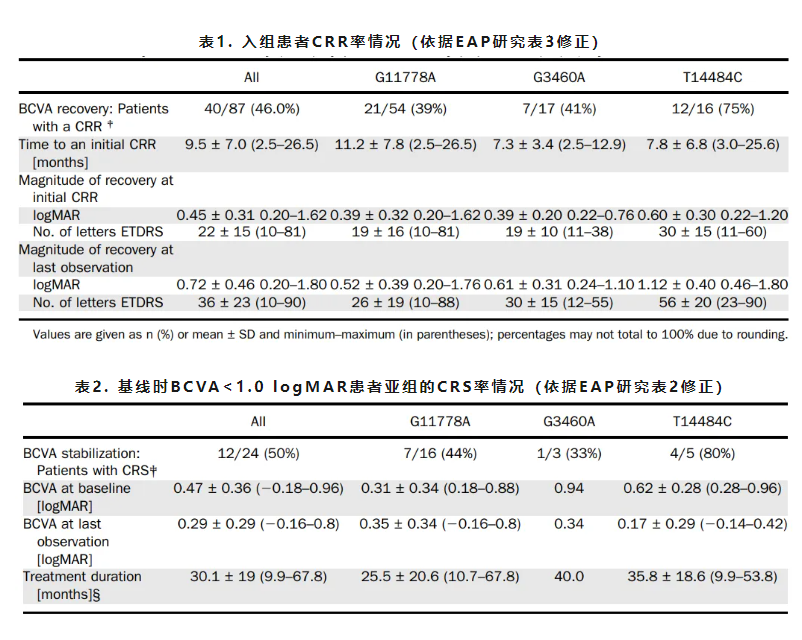
这些疗效数据显著超越了历史自然病程数据。对治疗反应的时间演化分析,更揭示了“长期主义”的至关重要性:仅45%的应答者在治疗开始后6个月内出现首次恢复;多达33%的应答者,其首次恢复出现在治疗6个月之后,部分患者甚至在治疗24个月后才开始显现改善迹象。总体趋势表明:治疗持续时间越长,实现恢复的患者比例越高,视力改善的幅度也越大。
这一“长期治疗,获益更佳”的结论,在后续设计更为严谨的IV期LEROS研究[4]中亦得到了明确验证。该研究通过设立匹配的自然史队列作为对照,发现艾地苯醌的治疗效果存在显著突变特异性:m.11778G>A突变患者在亚急性/动态期和慢性期均能获得显著获益;m.14484T>C突变患者在慢性期获益显著,亚急性/动态期获益不明显;m.3460G>A突变患者无论在哪个病程阶段,均未从艾地苯醌治疗中获益,甚至亚急性/动态期治疗后CRW率更高。这些结果充分证实了无论患者在亚急性/动态期(发病≤1年)抑或慢性期(发病>1年)启动艾地苯醌治疗,坚持为期24个月的长期疗程,均能获得持续累积的临床获益,打破了“慢性期治疗无效”的传统认知。综合上述高级别的循证医学证据,可凝练出当前LHON艾地苯醌治疗的核心策略:为最大化患者获得CRR的机会,治疗应尽早启动,并务必维持至少18-24个月。这既是为了给予药物足够的时间来“重启”处于功能休眠但结构尚存的RGCs,也是为了平稳度过可能出现的短暂“治疗谷底期”,最终引导视力步入持续改善的良性轨道。
专家点评
重塑认知,全程管理
以科学认知与战略耐心守护视觉之光
LHON 的治疗绝非“速决战”,而是一场需要科学认知与坚定耐心的持久战役。临床中最常见的误区,便是将治疗初期的“谷底”误认为治疗失败,进而中断方案,彻底丧失恢复机会。从疾病机制与研究证据来看,短暂视力降低是LHON动态恢复的正常生理性阶段,是 RGCs 从损伤静默到逐步唤醒的正常过程,医患双方都应建立理性预期。
其次,“早期干预、长期维持” 是 LHON 治疗的核心策略。艾地苯醌作为全球唯一获批的对因治疗药物,通过精准靶向线粒体损伤,实现“稳定残余视力、促进视力恢复” 的双重目标,彻底改变了 LHON“确诊即失明”的诊疗困境。相关研究等已确凿证实:早期启动并坚持 18~24 个月的规范长程治疗,能最大程度激活视神经修复潜能,提升 CRR 概率,显著改善视力并稳定残余视功能,尤其对 m.11778G>A 等预后较差的突变类型,长期治疗的获益更为显著。需注意的是,治疗效果存在突变依赖性,需结合患者突变类型制定个体化方案,例如对于m.3460G>A突变患者,需谨慎评估治疗价值,避免无效治疗[4,10]。
最关键的是,LHON 的诊疗需要医患同心、科学施策。临床医师应做好病程解读与用药宣教,帮助患者理解“谷底-恢复”规律;患者应摒弃焦虑、坚守疗程,不被短期视力波动干扰。总之,对于 LHON 患者而言,短暂的视力波动是康复的前奏,长期坚持才是恢复的关键。唯有以科学认知为指引,以耐心信心为支撑,完成足疗程规范治疗,才能真正守护视觉光路,穿越“视力谷底”,让更多青壮年患者重获清晰视界,迎来最终光明,回归正常生活。
小结
LHON 是线粒体突变驱动、遗传与环境共同作用的罕见致盲眼病,在我国,超十万青壮年患者深受其害。艾地苯醌的出现开启了对因治疗新时代,而治疗中“先降至谷底、再逐步恢复”是疾病固有规律,并非疗效不佳。EAP 研究与 LEROS 研究确凿证实:早期启动 ≥18–24 个月长程治疗,可最大化 CRR 概率,显著提升视力并稳定残余视功能;同时,治疗效果存在突变特异性,需结合患者突变类型制定个体化方案。总之,对于 LHON 患者而言,短暂的视力波动是康复的前奏,长期坚持才是恢复的关键。唯有科学认知病程、坚守规范治疗,才能穿越“视力谷底”,迎来最终光明。
参考文献
1.BARBONI P, et al. Am J Ophthalmol, 2023, 249: 99-107.
2.YU-WAI-MAN P, et al. J Med Genet, 2002, 39(3): 162-9.
3.YU-WAI-MAN P, et al. Am J Hum Genet, 2003, 72(2): 333-9.
4.Yu-Wai-Man et al., 2024, Cell Reports Medicine 5, 101437
5.Jia X, et al. J Hum Genet, 2006, 51 (10):851-856.
6.中华医学会医学遗传学分会遗传病临床实践指南撰写组. Leber遗传性视神经病变的临床实践指南[J]. 中华医学遗传学杂志,2020,37(3):284-288.
7.Meyerson C, et al. Clin Ophthalmol (2015) 9:1165–76.
8.ZhangYanqing,et al. (2025). Aging Medicine. 8. 624-633.
9.Li H,et al. J Genet Genomics. 2026 Feb 8:S1673-8527(26)00047-0.
10.Catarino CB, et al. J Neuroophthalmol. 2020 Dec;40(4):558-565.
11.KLOPSTOCK T, et al. A randomized placebo-controlled trial of idebenone in Leber's hereditary optic neuropathy [J]. Brain, 2011, 134(Pt 9): 2677-86.
声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
2 comments


 京公网安备 11010502033360号
京公网安备 11010502033360号
条评论
Linda Gareth
2015年3月6日, 下午2:51Donec ipsum diam, pretium maecenas mollis dapibus risus. Nullam tindun pulvinar at interdum eget, suscipit eget felis. Pellentesque est faucibus tincidunt risus id interdum primis orci cubilla gravida.