编者按:甲状腺相关眼病(TAO),作为Graves病最常见的甲状腺外表现,不仅影响患者的容貌和生活质量,严重时更可导致视力丧失,是临床医生面临的严峻挑战。在临床实践中,TAO的诊治常因涉及内分泌、眼科、影像科等多学科而变得碎片化,可能延误最佳治疗时机。在2025年8月1日~3日召开的第二十八次全军内分泌代谢病学术大会中,海军军医大学第二附属医院(上海长征医院)内分泌科石勇铨、李拓教授团队以“直面危象:重症甲状腺相关眼病的内外科协作与前沿探索”为题展开了精彩报告,分享了TAO的相关知识、经典案例,以及TAO诊疗多模态的前沿探索。现整理如下,以飨读者。

石勇铨 教授
上海长征医院
教授、博士生导师
上海长征医院内分泌科名誉主任学科带头人
中华医学会内分泌学分会委员
上海市医学会内分泌学分会主任委员
上海市医师协会内分泌代谢病分会副会长
解放军医学会内分泌分会常委
解放军医学会内分泌专业青年委员会主委
中初保内分泌专委会副主委
《中国内科年鉴》副主编

李拓 教授
上海长征医院
副主任医师、副教授、博士生导师
上海长征医院内分泌科行政副主任
上海市医学会内分泌学分会委员兼秘书、甲状腺学组组长
以第一/通讯作者在Cell Discov、Nat Comm、JCI等SCI杂志发表论文37篇
认识TAO:定义、临床表现及治疗
1.TAO的定义:器官特异性自身免疫性疾病
TAO又称Graves眼病,是一种与甲状腺疾病密切相关的、以眼眶及眶周组织炎性浸润为特征的器官特异性自身免疫性疾病[1]。TAO的常见症状包括:畏光流泪、异物感、刺痛、眼胀、眼球自发痛或活动痛,眼脸退缩红斑、结膜充血水肿、泪阜水肿、眼球突出、眼球活动障碍,斜视、复视、暴露性角膜病变和视神经病变,甚至失明(图1)。此外,由于外观的改变和视功能的损害,TAO患者常伴有显著的焦虑、抑郁等精神心理问题,生活质量受到严重影响。
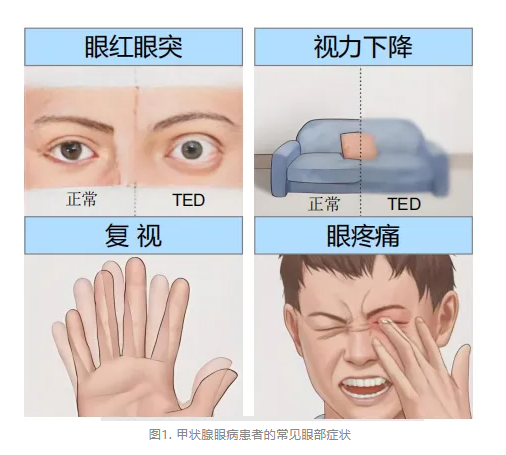
2.TAO的治疗:疾病状态是依据
TAO患者临床结局差异较大——轻度患者目前并不强调直接干预,以观察为主;中至重度或危及视力者需尽早接受TAO的干预治疗[2-4]。对TAO患者进行准确、全面的评估是制定个体化治疗方案的基石,评估主要围绕“临床活动性”和“疾病严重程度”两个维度。
临床活动性评分:判断TAO是否处于炎症活动期的关键指标(CAS),而活动期是免疫抑制治疗的最佳窗口期。初诊7分法(1项计1分,≥3分为活动期):自发性眼球后疼痛、眼球运动时疼痛、眼睑充血、眼睑水肿、结膜充血、结膜水肿、泪阜肿胀。复诊10分法(≥4分为活动期):在初诊7分法基础上增加突眼度增加>2mm、眼球运动下降≥8°、视力减退(Snellen视力表下降≥1行)。
疾病严重程度分级:欧洲Graves眼病协作组(EUGOGO)提出的分级标准因其简明扼要、易于临床应用而被广泛采纳。该标准将TAO分为三级,直接指导治疗决策(表1)。EUGOGO标准对视神经受累和角膜溃疡等严重体征给予足够重视,便于临床及时诊断和采取紧急措施抢救视功能[5]。
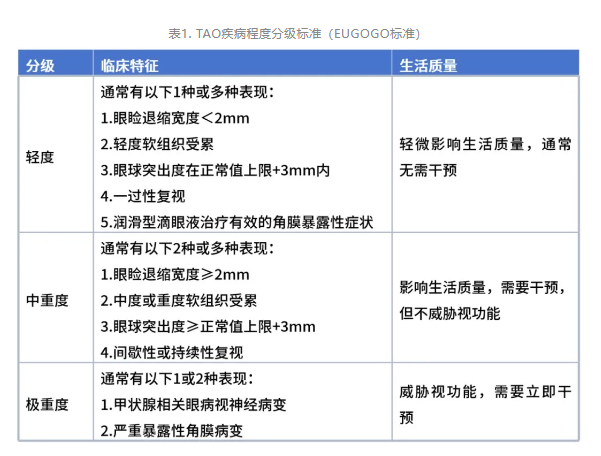
3.中重度以上TAO患者受治疗条件约束较大
TAO的治疗决策是一个综合性过程,需全面考虑疾病的活动性与严重程度、病程、治疗效果、安全性、费用、药物可及性以及患者的个人意愿。总体而言,治疗策略因人而异,遵循分级管理的原则(表2)[5]。

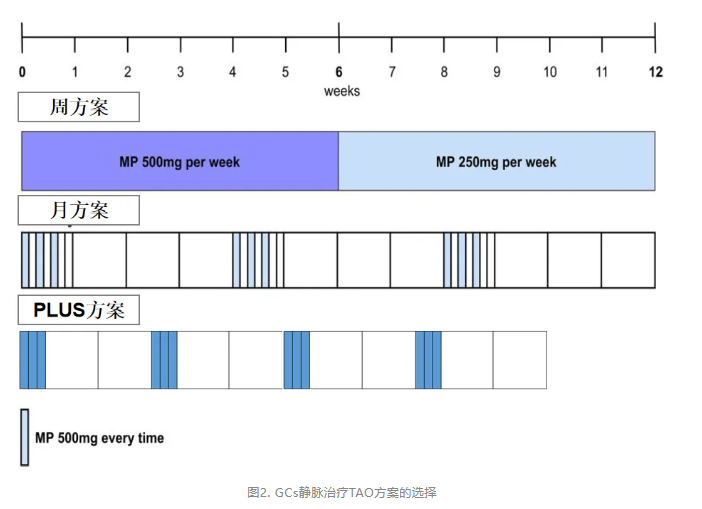
糖皮质激素(GCs)凭借其强大的抗炎和免疫抑制作用,是目前国内外指南一致推荐的治疗中重度活动期TAO的一线药物,能有效减轻眼眶组织的炎症反应,改善软组织体征。GCs静脉治疗方案的选择较多(见图2):
①标准周方案(累积4.5 g):甲泼尼松龙0.5 g静脉滴注,每周1次,共6周,继而甲泼尼龙0.25 g静脉滴注,每周1次,共6周。
②改良月方案(累积4.5 g):沈洁教授团队RCT研究[6]表明,采用月治疗方案(每月3次,隔天给药,每次0.5 g,共3个月)也可达到相似的治疗效果。另一前瞻性非随机单中心研究,采用改良的月治疗方案也得到相似的结果。
③高剂量周方案(累积7.5g):甲泼尼龙0.75 g静脉滴注,每周1次,共6周,继而甲泼尼龙0.5 g静脉滴注,每周1次,共6周。用于伴有严重眼部软组织病变、严重眼球突出或复视的病情复杂的中重度活动期TAO。
④PLUS冲击方案(累积6~12 g):石勇铨教授团队采用的方案是,甲泼尼龙0.5 g静脉滴注/d,连续3天,间隔14~21天,共4次,累积6 g阶段性评估。其累计周期短、不良反应低,更常用于伴有严重眼部软组织病变、严重眼球突出或复视的病情复杂的中重度活动期TAO。
案例回顾:1例重症TAO的诊断与治疗
1.患者基本情况
患者王先生,50岁,因“双眼畏光流泪伴复视9月余”入院。初见时,患者用手遮挡左眼,表情痛苦。
2.初步诊疗:眼科的视角
患者自述2024年1月起出现左眼突出、充血,双眼睑肿胀,伴有眼球活动痛、眼涩、畏光等,5月症状加重。发病前15个月前确诊“Graves病、甲状腺功能亢进”,长期接受抗甲亢药物治疗,但依从性不佳。当地眼科初步考虑为“病毒性角膜炎”,多次给予局部激素治疗,但效果甚微。
3.转诊:内分泌科的深入探查与鉴别诊断
由于患者症状持续恶化且有明确的甲亢病史,被转诊至内分泌科进一步诊治。内分泌科医生在接诊后,重新详细询问了病史,将主诉修正为“心慌、手抖15月,复视伴眼球突出9月”,并梳理出一条更清晰的疾病发展时间线:
2023年3月:出现心慌、手抖、怕热、体重下降等典型甲亢症状,确诊Graves病,开始甲巯咪唑片治疗,但甲功控制不理想。
2023年8~10月:相继出现右眼视力下降和复视,未予重视。
2024年1月:眼球突出、红肿等炎症表现加剧。
2024年4月:因甲功化验提示甲减而自行停用抗甲亢药物,导致病情波动。
2024年5月:眼部症状进行性恶化,出现眼睑闭合不全。
基于患者典型的甲亢病史和眼部表现,高度怀疑TAO。然而,对于单侧或不对称性眼球突出,必须进行严谨的鉴别诊断,以排除其他严重疾病,遵循“一元论”原则,谨慎排除他症风险——眼眶肿瘤、眼眶炎性假瘤、颈动脉-海绵窦瘘、Wegener肉芽肿等系统性血管炎、颅内占位性病变、重症肌无力。
4.最终诊断:TAO(CAS 7分,极重度)
经过全面的体格检查和辅助检查,最终诊断明确:
TAO:患者出现角膜暴露(角膜脱落)、眼睑闭合不全、双眼视力下降至0.3,根据EUGOGO分级标准,严重程度评定极重度/威胁视力。患者存在双侧球结膜水肿充血、眼睑水肿、泪阜肿胀、自发性眼球后痛和眼球运动痛,CAS评分为7分(活动期)。甲状腺功能检查证实甲亢未控制,甲状腺相关抗体(TPO-Ab, TG-Ab, TR-Ab)阳性。眼部B超显示双眼眼外肌弥漫性增粗。突眼度测量为右眼23 mm,左眼20 mm。
Graves病,甲状腺功能亢进症。
继发性骨质疏松症(甲状腺功能亢进症相关)。
5.制定综合治疗方案
针对患者极重度、活动期TAO合并甲亢的危重情况,多学科团队制定了综合的治疗方案:
甲亢治疗:使用甲巯咪唑片控制甲状腺激素合成,并用β-受体阻滞剂(美托洛尔)缓解心悸等高代谢症状。
TAO核心治疗:立即启动大剂量静脉激素冲击疗法(甲泼尼龙500 mg/日,静脉滴注,连续3天,连续2周强化治疗),以迅速控制眼眶炎症,挽救视力。
眼部支持与保护:使用小牛血去蛋白提取物眼膏保护角膜,并进行外睑减张处理,防止角膜进一步损伤。
激素不良反应预防性治疗:同时给予抑酸药(奥美拉唑)、胃黏膜保护剂(铝碳酸镁)、补钾(氯化钾缓释片)及镇静药物(地西泮),以预防和处理激素的潜在副作用。
骨质疏松治疗:给予双膦酸盐、活性维生素D和钙剂,防治骨量丢失。
经过上述综合干预,患者的眼部炎症和全身症状得到了显著控制。眼部充血、水肿明显消退,眼球活动疼痛缓解,为后续的康复治疗创造了条件(图3)。这一案例充分体现了在面对重症TAO时,早期识别、准确评估以及内分泌科、眼科等多学科紧密协作的极端重要性。

前沿探索:人工智能在TAO诊疗中的应用
尽管临床评估和传统影像学在TAO诊疗中发挥着核心作用,但仍存在主观性强、无法精确定量等局限。构建客观、可推广的预测模型,对于实现个体化精准治疗意义重大。
1.基于AI的三维参数获取与模型构建
传统影像学评估多依赖于二维参数,而眼眶是一个复杂的三维结构。三维参数能更准确地反映病理变化,但手动勾画耗时耗力,且一致性差。人工智能(AI)技术的发展为解决这一难题提供了可能。
上海长征医院内分泌科团队与影像科团队利用深度学习算法(nnU-Net)[7],通过200例TAO患者的MRI数据完成基于AI技术的三维ROI勾画及体积测算工具的训练,可快速、精准地获取各条眼外肌、泪腺、眶后脂肪、视神经等不规则物体的三维体积参数及信号强度。该AI工具仅需约120秒即可完成一个MRI序列的初步勾画,与经验丰富的影像医师相比,其ROI限定准确率高达93.9%,极大地提升了评估效率和客观性。
2.AI模型的诊断效能评估
团队进一步评价了基于AI获取的三维参数用于诊断TAO活动性和严重程度的效能。结果显示,在51例活动期与49例非活动期TAO患者中,结合了“眼外肌体积”和“信号强度”的多参数模型(Model 3)展现出最高的诊断效能,其ROC曲线下面积(AUC)优于单一参数模型;在14例轻度与86例中重度TAO患者中,同样是多参数模型(Model 3)表现最佳,能有效区分不同严重程度的患者(图4)。这表明基于AI的定量三维影像学分析,有望成为评估TAO病情的强大客观工具。
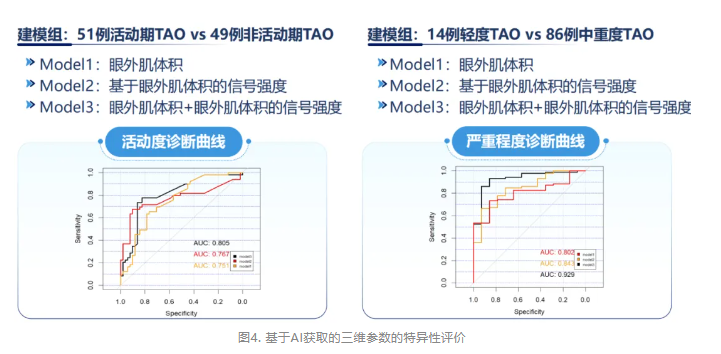
未来的终极目标是构建一个整合临床信息、实验室检查以及AI影像学参数等的多模态预测模型。这样的模型不仅能辅助诊断,更有可能预测疾病进展、治疗反应和远期预后,从而真正实现TAO的个体化、精准化管理。
结语:TAO是一种复杂的自身免疫性疾病,其临床管理面临严峻挑战。TAO的治疗需综合评估病程、分期分级、治疗效果、安全性、费用、药物可及性及患者意愿,并据此制定个体化方案。针对极危重度活动期TAO,治疗原则必须严格把握时间窗,以免疫调节与改善症状体征为核心目标。糖皮质激素作为国内外指南和共识推荐的治疗手段,虽存在一定风险,但通过治疗过程中的密切评估与联合外科干预,可显著提升疗效并降低潜在风险。
参考文献:
1. Bartalena L.J Endocrinol Invest.2014 Aug;37(8):691-700.
2. Tanda ML,et al. J Clin Endocrinol Metab. 2013 Apr;98(4):1443-9.
3. Menconi F, et al. Thyroid. 2014 Jan;24(1):60-6.
4. Piantanida E, et al. J Endocrinol Invest. 2013 Jun;36(6):444-9.
5. 中国甲状腺相关眼病诊断和治疗指南,中华眼科杂志2022 年9 月第58 卷第9 期.
6. Li Z, Shen J,et al. J Clin Endocrinol Metab. 2023 Dec 21;109(1):36-45.
7. Zwijnen AW. Comput Biol Med . 2024 Sep:179:108853.
声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
2 comments

 京公网安备 11010502033360号
京公网安备 11010502033360号
条评论
Linda Gareth
2015年3月6日, 下午2:51Donec ipsum diam, pretium maecenas mollis dapibus risus. Nullam tindun pulvinar at interdum eget, suscipit eget felis. Pellentesque est faucibus tincidunt risus id interdum primis orci cubilla gravida.