编者按:神经炎症依赖于神经胶质细胞的炎症反应,这已成为青光眼神经退行性变病因学的一个重要组成部分。尽管神经胶质反应具有早期适应性和修复性特征,但神经胶质细胞连同周围免疫细胞的长期炎症反应,对视网膜神经节细胞(RGC)轴突和突触产生广泛的毒性。近期,有研究人员综述了青光眼神经炎症的最新研究进展,重点介绍了参与神经胶质反应的细胞内外因素、炎症途径与线粒体途径之间的相互依赖性、研究方向对未来的免疫调节治疗具有启发意义。
困境:青光眼视神经病变机制仍不明确
青光眼是导致不可逆转失明的主要原因,目前全世界约有8000万人患有青光眼。据估计,到2040年,患有青光眼致盲疾病的人数预计将超过1亿。青光眼患者的视觉功能逐渐丧失与RGC的退行性病变有关,其特征是视网膜体细胞凋亡、视神经轴突变性以及树突和轴突终末的突触丧失。实验研究的结果表明,青光眼的RGC变性由相关的致病过程驱动,包括生物力学、血管、代谢、氧化和炎症反应等多种因素。目前人们对青光眼视神经退行性变的分子认识尚不完全,青光眼的治疗主要依赖于降低眼压,然而,即使有效控制了眼压,部分疾病也会持续进展。人们普遍认为,除了眼压外,还有其他多种因素影响青光眼中RGC的存活,青光眼视神经退行性变是多种触发因素、多种细胞类型和多种分子途径的复杂相互作用的结果。近年来,多位学者进行了多项关于青光眼中胶质细胞驱动的神经炎症的分子研究进展,特别强调了星形细胞-小胶质细胞在炎症反应中的协调作用、调节神经炎症的细胞内外因素、炎症和线粒体病因途径之间的相互依赖性,研究为青光眼的免疫调节治疗提供了潜在的启示。
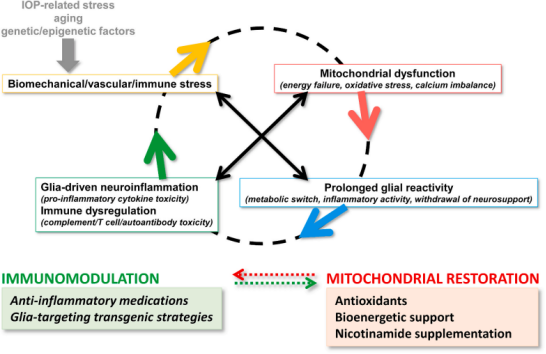
图1. 青光眼视神经退行性变的汇聚性病因
参与神经炎症的胶质细胞亚型:星形胶质细胞、少突胶质细胞
胶质细胞(包括星形胶质细胞和小胶质细胞)参与了RGC的健康维持和疾病发生,对健康状态起到决定性作用。神经胶质细胞能够检测到青光眼相关的应激以及应激或受损的RGC产生的危险信号,并作出反应。虽然早期神经胶质反应包含了适应和修复因子,以消除或抑制致病因素,但这种状态不能长期维持。青光眼中持续的组织应激可以促使神经胶质细胞发生炎症反应和神经退行性病变。
星形胶质细胞在维持视网膜和视神经组织稳态方面起着重要作用。
星形胶质细胞突起包裹着RGC体和轴突,并提供结构支持,对于克服与眼内压相关的生物力学应激特别重要。
通过清除细胞碎片,星形胶质细胞还可以促进组织愈合,这与它们在青光眼病程中增强的吞噬活性有关。
星形胶质细胞还参与了RGC突触的形成、成熟、维护和突触传递。
星形胶质细胞是神经血管单元的组成部分,通过调节神经血管耦合来满足RGC的动态代谢需求,以保持突触活性。
除了血流调节,星形胶质细胞与神经血管单元其他成分的相互作用,主要包括血管内皮,在维持血脑屏障的紧密连接特性中发挥关键作用。
星形胶质细胞与其周围的免疫细胞相互作用,以维持视网膜和视神经组织的内稳态。
与Müller胶质细胞一样,少突胶质细胞值得青光眼研究人员更多的关注,以进一步研究其在青光眼神经退行性变和神经炎症中的作用。
存在于视神经乳头后面的髓鞘化少突胶质细胞除了维持轴突的完整性外,还为轴突提供代谢支持。
少突胶质细胞可能不直接参与炎症反应,然而,它们可作为炎症损伤的目标。在青光眼中,胶质细胞介导的脱髓鞘甚至可能先于轴突消失。
少突胶质细胞作为免疫细胞浸润视神经的物理屏障作用也可能发生功能障碍和结构改变。
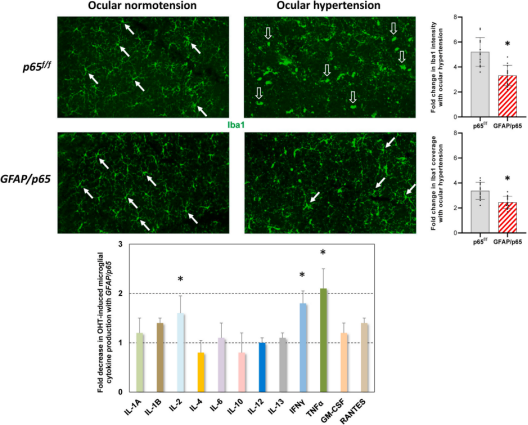
图2. 星形胶质细胞和小胶质细胞关系密切
青光眼炎症病变的分子机制
转录组学和蛋白质组分析的最新研究发现,对人类供体眼睛或青光眼动物模型进行相关分析后,许多参与炎症途径的分子在青光眼早期表达增加。研究的分子包括传感器和诱导因子(如模式识别受体、TLRs或NLRs)、传感器和调节因子(如MyD88、MAPKs、NF-κB)、炎症信号的放大因子和效应因子(如细胞因子和趋化因子)。
星形胶质细胞对微环境非常敏感,可通过机械敏感离子通道直接感知眼内压相关的机械应变。炎症反应性的刺激也可能介导由泛链蛋白通道和嘌呤能受体共同介导的机械敏感途径。在青光眼中,除了眼压相关应激的机械感觉外,RGC固有或外源性的各种其他因素也可以通过嘌呤能受体或TLR信号诱导神经胶质炎症反应。
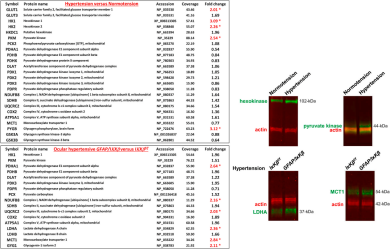
图3. 青光眼模型实验小鼠的星形胶质细胞在代谢变化中的研究
值得注意的是,衰老是青光眼细胞应激的另一个因素,年龄可促使免疫系统表达促炎特征,发生炎症反应。事实上,老年大脑中的小胶质细胞可启动一些与年龄相关的神经退行性疾病中的慢性炎症,星形胶质细胞也表现出与年龄相关的促炎变化,这对年龄相关突触丧失和神经炎症具有重要意义。这种与年龄相关的改变可能与青光眼的神经炎症有关。
关于青光眼神经退行性变的血管应激相关成分,多项研究发现,在人类青光眼和动物模型中,视网膜和视神经乳头的内皮素表达增加,通过应用内皮素受体拮抗剂抑制内皮素信号通路,可保护青光眼模型小鼠免受青光眼损伤。关于神经炎症,大鼠玻璃体内注射内皮素-1可诱导视网膜产生促炎细胞因子,并可引起短暂的视网膜血管收缩、缺氧和介导的RGC死亡,这也可能作为神经炎症的代谢调节因子参与青光眼疾病的发生发展。
青光眼中胶质细胞的早期反应表现为促炎细胞因子的增加,如TNFα、IFNγ、IL-1、IL-2、IL-12和趋化因子。胶质细胞产生的促炎细胞因子作为炎症程序的放大器和炎症神经毒性的效应器:一方面,趋化因子吸引更多的免疫细胞,这一过程促进了其他促炎分子的分泌,从而加剧了神经炎症;其他分子如ROS或iNOS,也会放大炎症并导致损害。与此同时,其他一些分子提供反调控,以减弱炎症的诱导物或放大器。与抗炎细胞因子的产生相反,促炎细胞因子产生的规模和持续时间的相对失衡导致了神经炎症的形成。细胞因子受体表达的平行改变也是炎症结局的决定性因素。随着青光眼视网膜和视神经中促炎细胞因子胶质细胞分泌的增加,青光眼房水和血液样本中这些细胞因子的水平随之增加。
总结
青光眼神经炎症的最新研究表明,与IOP相关的生物力学和血管应激、老化、RGC损伤、遗传和表观遗传易感性可能共同损害青光眼视网膜和视神经的神经胶质免疫调节功能。因此,尽管神经胶质反应存在早期适应性和修复性,长期炎症反应的神经胶质和外周免疫细胞导致视神经发生退行性病变。炎症毒性对RGC轴突、小体、树突状树和脑突触存在广泛影响的相关证据,为神经炎症的治疗调节提供了越来越多的希望。
参考文献:Tezel Gülgün.(2022). Molecular regulation of neuroinflammation in glaucoma: Current knowledge and the ongoing search for new treatment targets. Prog Retin Eye Res, 87(undefined), 100998. doi:10.1016/j.preteyeres.2021.100998














 京公网安备 11010502033360号
京公网安备 11010502033360号
条评论
Linda Gareth
2015年3月6日, 下午2:51Donec ipsum diam, pretium maecenas mollis dapibus risus. Nullam tindun pulvinar at interdum eget, suscipit eget felis. Pellentesque est faucibus tincidunt risus id interdum primis orci cubilla gravida.